Lợi ích của công cụ này chính là bạn có thể tạo ra những sửa đổi tạm thời, giúp cho chỉnh sửa gen trở thành việc an toàn hơn nhiều so với trước đây. Các nhà nghiên cứu cho biết hệ thống mới mang tên REPAIR có thể hoạt động tương đối hiệu quả ở tế bào người.
Trong tương lai, kỹ thuật này có thể được dùng để trị bệnh cũng như hiểu rõ hơn về vai trò của ARN trong việc gây ra những căn bệnh đó. 'Nó là một công cụ khác trong hộp dụng cụ mà trước đây chúng tôi chưa từng có”, Mitchell O’Connell, trợ lý giáo sư thuộc Khoa Hoá sinh và Sinh lý học tại đại học Rochester, người không tham gia vào nghiên cứu, cho biết. “Việc này giống như bạn phát triển một công nghệ cho phép bạn nhìn thấy những điều chưa từng thấy trước đó, hoặc điều chỉnh những thứ không thể điều chỉnh”.
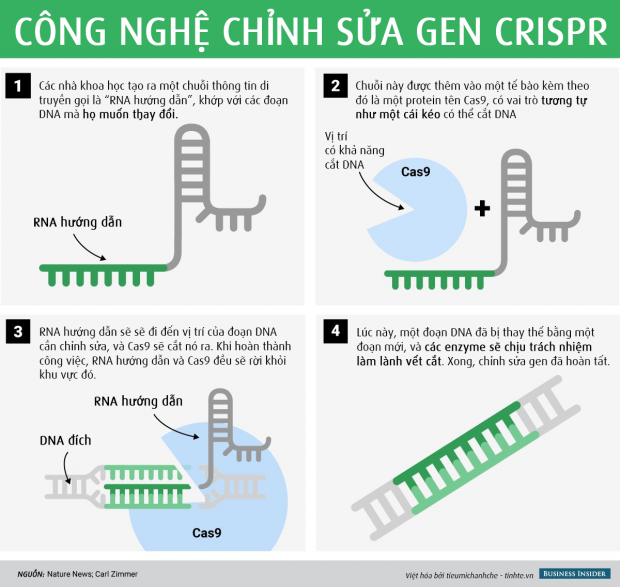
Kỹ thuật chỉnh sửa gen CRISPR được phát triển dựa trên cơ chế phòng vệ dùng vi khuẩn để ngăn chặn virus bằng cách cắt đứt ADN của chúng sau đó dán vào nơi khác. Nhờ công cụ này, các nhà khoa học đã tạo ra cơ chế nhằm tinh chỉnh ADN để tạo ra những con ong cơ bắp hoặc muỗi không truyền bệnh sốt rét. Nhưng CRISPR bản thân nó cũng có nhiều loại khác nhau để dùng cho các mục đích khác nhau. Công cụ chỉnh sửa gen được ứng dụng nhiều nhất và phổ biến nhất cho đến hiện tại chính là CRISPR-Cas9.
CRISPR được sử dụng trong nghiên cứu mới là CRISPR-Cas13. Thay vì tác động đến ADN, dạng CRISPR này lại nhắm tới một loại phân tử sinh học quan trọng khác có thể được tìm thấy trong bất kể dạng sự sống nào: ARN. Phần lớn dòng đời, ARN tồn tại bên trong cơ thể để giúp ADN xây dựng các protein. Và protein lại đóng một vai trò quan trọng trong việc gây ra bệnh. David Cox, một nghiên cứu sinh tại phòng thí nghiệm Zhang ở Viện Broad (đối tác của MIT và Đại học Harvard), đồng tác giả của nghiên cứu cho rằng chỉnh sửa ARN mang một lợi thế nếu so với chỉnh ADN. ARN liên tục được tạo ra và tái sử dụng bên trong tế bào, do đó, sửa ARN không để lại những tác động vĩnh viễn.
Mặc dù vậy, những thay đổi tạo ra trong ARN vẫn có thể mang đến hiệu quả nhất định: hệ thống CRISPR có thể tồn tại trong tế bào một khoảng thời gian, chẳng hạn như vài tháng, cho phép kéo dài thời gian chỉnh sửa ARN khi nó hình thành. Điều này giúp toàn bộ quá trình trở nên an toàn hơn. Ví dụ trong trường hợp xấu, việc chỉnh sửa ARN mắc lỗi, ARN lỗi đó sẽ bị phân huỷ trong vòng 24 tiếng. Tuy nhiên nếu bạn gặp điều tương tự khi chỉnh ADN thì lỗi đó không thể đảo ngược và có thể gây nên những hậu quả nghiêm trọng như ung thư.
Một vài thay đổi trong ADN có thể di truyền cho cả thế hệ sau trong khi thay đổi ở ARN nhìn chung không di truyền. Từ trước đến nay, các nhà khoa học xem chỉnh sửa gen là một công cụ vô cùng mạnh mẽ trong việc giải quyết rất nhiều vấn đề, kể cả những vấn đề phức tạp nhất của y học. Nhưng bên cạnh đó, họ lúc nào cũng tỏ ra đề phòng với những hậu quả không thể lường trước được nếu phạm sai lầm trong quá trình tác động đến tự nhiên. Giờ đây, tạo ra công cụ có thể chỉnh sửa ARN mang đến cho chúng ta một “chiến lược an toàn hơn, đặc biệt là đối với những thứ mà bạn không muốn thay đổi vĩnh viễn”, theo O’Connell.
Để tạo ra công cụ mang tên REPAIR này, các nhà nghiên cứu đã kết hợp CRISPR-Cas13 với một protein gọi là ADAR. Nguyên lý hoạt động như sau: enzym Cas13 được lập trình để tìm kiếm một trình tự ARN cụ thể có thể tương ứng với một đột biến gây bệnh; protein ADAR sau đó sẽ làm nhiệm vụ chỉnh sửa. Trải qua các thử nghiệm, các nhà nghiên cứu cho biết hiệu quả của công cụ mới trong việc chỉnh sửa ARN từ 20 - 40% và có thể lên đến 90% trong một số trường hợp nhất định. Đôi khi, hệ thống cũng mắc sai lầm.
Dù công cụ chỉnh gen hiện nay rất chính xác nhưng có lúc nó lại cắt nhỏ những đoạn mà di truyền mà chúng không được tạo ra để cắt. Sai lầm nhỏ này có thể đưa đến những hậu quả nguy hiểm và các nhà khoa học muốn đảm bảo giảm số lần cắt sai xuống càng thấp càng tốt. Phiên bản đầu tiên của công cụ mới sai phạm 20.000 lần, theo Omar Abudayyeh, đồng tác giả của nghiên cứu cho biết. “Đó là khoảnh khắc đáng thất vọng”, ông nói. Nhưng sau đó, những điều chỉnh của các chuyên gia giúp công cụ hoạt động hiệu quả hơn, số lần cắt sai giảm xuống còn 10-20 lần ở mỗi vị trí mục tiêu, giúp cho nó trở nên an toàn và chính xác hơn.
O'Connell cho biết ông cảm thấy rất ngạc nhiên bởi hệ thống hoạt động tốt như vậy. Trước đây, ARN từng được nhắm đến trong một số nỗ lực nhằm giúp thuốc hiệu quả hơn trong việc trị bệnh, theo ông. Nhưng nhờ hệ thống CRISPR mới, việc điều trị những căn bệnh nguy hiểm đến tính mạng như hemophilia hay bệnh cơ tim phì đại (có thể dẫn đến đột tử) trở nên dễ dàng hơn. Trước khi điều đó xảy ra, việc cần làm trước mắt là phải tối ưu hoá công cụ này, giúp nó hoạt động chính xác hơn.
Các nhà nghiên cứu cũng cần chứng minh mức độ hiệu quả của kỹ thuật mới trên cơ thể động vật, trước khi nó được áp dụng trên cơ thể người. “Việc biến nó trở thành một liệu pháp điều trị thật sự là một chặng đường rất dài”, Jonathan Gootenberg, đồng tác giả của nghiên cứu, chia sẻ. Công cụ mới này và CRISPR-Cas9 rõ ràng có tiềm năng để cách mạng hoá cách chúng ta điều trị bệnh. Và đó cũng là động lực giúp Gootenberg, Cox hay Abudayyeh luôn làm việc một cách miệt mài tại phòng thí nghiệm Zhang Lab.
Abudayyeh khi còn học trung học từng chứng kiến một người phụ nữ mắc ung thư phổi giai đoạn cuối và có lẽ chỉ còn sống được vài tháng. “Bạn cảm thấy hoàn toàn bất lực trong tình huống đó bởi bạn không thể làm gì, ngay khi bạn là một bác sĩ”. Đó là động lực khiến ông quyết tâm theo đuổi ngành công nghệ sinh học. “Bạn sẽ cảm thấy như được trao một quyền lực gì đó khi bạn ở trong phòng thí nghiệm, chỉ cần suy nghĩ về những phương pháp mới để tạo ra các công nghệ đầy tiềm năng để giúp đỡ những bệnh nhân như thế. Thật sự rất tuyệt vời”.
Nguồn: The Verge, Ảnh: Phys.org









![Review Trên tay củ sạc nhanh Zendure Superport S3Pro – 65w [2 Type C + 1 Type A] model 2021](http://cdn.trangcongnghe.vn/thumb/160x240/2021-06/danh-gia-thiet-bi-so_review-tren-tay-cu-sac-nhanh-zendure-superport-s3pro-65w-2-type-c-1-type-a-model-2021-1.jpg)
