- Dữ liệu Giai đoạn 2 nhấn mạnh tiềm năng hàng đầu trong phân khúc của thuốc kích thích kép GLP-1R/GIPR BGM0504 trong quản lý cân nặng và giảm nguy cơ chuyển hóa ở bệnh nhân tiểu đường loại 2 và những người thừa cân nhưng không béo phì
- Dữ liệu tiền lâm sàng của BGM1812 hỗ trợ việc phát triển tiếp theo như một analog amylin thế hệ mới để điều trị béo phì
TÔ CHÂU, TRUNG QUỐC, NGÀY 24 THÁNG 6 NĂM 2025 /PRNewswire/ -- BrightGene Pharmaceutical Co., Ltd., một công ty dược phẩm quốc tế định hướng đổi mới, đã trình bày dữ liệu từ hai nghiên cứu Giai đoạn 2 cho BGM0504, loại thuốc thử nghiệm kích thích kép nhắm vào thụ thể peptide giống glucagon-1 (GLP-1R) và thụ thể polypeptide kích thích insulin phụ thuộc glucose (GIPR), cùng với dữ liệu tiền lâm sàng cho analog amylin mới, BGM1812, tại Hội nghị Khoa học lần thứ 85 của Hiệp hội Tiểu đường Hoa Kỳ (ADA).
Kết quả từ hai nghiên cứu Giai đoạn 2 riêng biệt của BGM0504 cho thấy tiềm năng đáng kể trong quản lý cân nặng và giảm nguy cơ chuyển hóa ở bệnh nhân tiểu đường loại 2 (bao gồm ưu thế so với semaglutide), và ở những người thừa cân hoặc béo phì nhưng không mắc tiểu đường. Dữ liệu tiền lâm sàng của BGM1812 cho thấy khả năng hoạt hóa thụ thể vượt trội, giảm cân mạnh mẽ và tiềm năng hiệp đồng với hoạt hóa kép GLP-1/GIP, hỗ trợ phát triển loại thuốc này như một analog amylin thế hệ mới để điều trị béo phì.
'Những dữ liệu Giai đoạn 2 này làm nổi bật tiềm năng hàng đầu trong phân khúc của BGM0504 như một phương pháp điều trị bệnh tiểu đường loại 2 và béo phì, bao gồm khả năng vượt trội so với semaglutide và hồ sơ an toàn mạnh mẽ, trong khi dữ liệu tiền lâm sàng của chúng tôi về BGM1812 hỗ trợ việc phát triển liên tục như một analog amylin thế hệ mới để điều trị béo phì, nhấn mạnh thêm triển vọng trong danh mục sản phẩm của chúng tôi,' ông Jiandong Yuan, CEO của BrightGene cho biết. 'Dựa trên chuyên môn sâu rộng về peptide và di sản vững chắc trong phát triển thuốc hiệu quả và chất lượng cao, BrightGene cam kết thúc đẩy nhanh các liệu pháp đổi mới nhằm đáp ứng nhu cầu chưa được đáp ứng của bệnh nhân trong bệnh chuyển hóa và các lĩnh vực điều trị quan trọng khác.'
Nghiên cứu Giai đoạn 2 BGM0504 ở bệnh nhân Tiểu đường Loại 2
Nghiên cứu đa trung tâm, ngẫu nhiên, mù đôi (có đối chứng với giả dược) và nhãn mở (có đối chứng tích cực với semaglutide) này đánh giá dược động học, độ an toàn và hiệu quả của việc tiêm dưới da hàng tuần BGM0504 dựa trên tiêu chí chính là thay đổi HbA1c so với ban đầu tại Tuần thứ 12 sử dụng liều mục tiêu, và nhiều tiêu chí phụ bao gồm PPG-2 giờ, FPG, cân nặng, HbA1c và tỷ lệ đạt mục tiêu kết hợp HbA1c/cân nặng, HOMA2-B, lipid máu, huyết áp tâm thu (SBP) và huyết áp tâm trương (DBP).
Nghiên cứu đã tuyển chọn 67 người tham gia mắc tiểu đường loại 2 trong độ tuổi từ 18 đến 65, trong đó 64 người đã nhận liều thuốc sau khi phân nhóm ngẫu nhiên, được phân ngẫu nhiên thành năm nhóm: 5mg (n=13), 10mg (n=12), 15mg (n=13), nhóm đối chứng tích cực (semaglutide; n=16) hoặc giả dược (n=13). Những người tham gia bao gồm người lớn có HbA1c ban đầu trong khoảng từ 7,0% đến 10,0% và chỉ số khối cơ thể (BMI) từ 19,5 đến 35 kg/m2.
Tại Tuần thứ 12 sử dụng liều mục tiêu, điều trị với BGM0504 dẫn đến giảm HbA1c trong cả ba nhóm liều lượng, với sự khác biệt có ý nghĩa thống kê so với nhóm giả dược và lớn hơn so với điều trị bằng semaglutide, bao gồm -1,72% ở nhóm 5mg, -1,94% ở nhóm 10mg và -2,48% ở nhóm 15mg, so với -1,43% của semaglutide và -0,28% của giả dược. Kết quả tương tự cũng được ghi nhận trong nhiều tiêu chí phụ, bao gồm PPG-2 giờ, FPG, cân nặng vàHbA1c và tỷ lệ đạt mục tiêu kết hợp HbA1c/cân nặng, trong khi các xu hướng cải thiện khác nhau được quan sát thấy ở HOMA2-B, lipid máu, SBP và DBP. Hầu hết các tác dụng phụ xuất hiện trong quá trình điều trị (TEAE) đều ở mức độ 1 hoặc 2 trong giai đoạn chỉnh liều nhanh và dần được dung nạp sau khi đạt đến liều mục tiêu. Các tác dụng phụ đường tiêu hóa liên quan đến điều trị phổ biến nhất là tiêu chảy, buồn nôn và chướng bụng; không ghi nhận phản ứng hạ đường huyết hoặc các tác dụng phụ bất ngờ khác.
Nghiên cứu Giai đoạn 2 BGM0504 trong béo phì
Nghiên cứu ngẫu nhiên, mù đôi, có đối chứng giả dược này đánh giá độ an toàn và hiệu quả của BGM0504 ở 120 người trưởng thành Trung Quốc bị béo phì trong quá trình dùng nhiều liều (tiêm dưới da). Những người tham gia bao gồm người trưởng thành có BMI ≥ 24kg/m2 (BMI trung bình tại thời điểm sàng lọc ≥ 27kg/m2) kèm tiền đái tháo đường và/hoặc ít nhất một bệnh lý đi kèm liên quan đến béo phì, hoặc người trưởng thành bị béo phì (BMI ≥ 28kg/m², BMI trung bình tại thời điểm sàng lọc ≥ 30kg/m²). Những người tham gia được phân ngẫu nhiên vào bốn nhóm: 5 mg (n=30), 10 mg (n=30), 15 mg (n=30), hoặc giả dược (n=30). Nghiên cứu bao gồm giai đoạn chỉnh liều (2-6 tuần), điều trị trong 24 tuần với liều hàng tuần, và theo dõi trong 2 tuần.
Kết quả nghiên cứu cho thấy giảm vòng eo từ −8,0 cm đến −12,98 cm (p < 0,001), và giảm cân đáng kể từ -10,77% đến -19,78% (trung bình LS, đã điều chỉnh theo giả dược). Kết quả cũng cho thấy cải thiện huyết áp tâm thu từ −11,60 đến −13,03 mmHg và huyết áp tâm trương từ −5,98 đến −7,50 mmHg (p < 0,05).
Các chỉ số phụ tiếp tục củng cố hiệu quả của BGM0504 và tất cả các liều đều được dung nạp tốt với các tác dụng phụ phổ biến.
Nghiên cứu tiền lâm sàng BGM1812
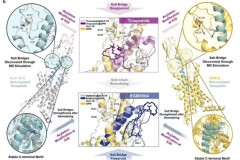
Trong một nghiên cứu tiền lâm sàng, BGM1812 cho thấy hoạt hóa thụ thể mạnh với hoạt tính kích thích tăng 1,8× và 2,2× (EC50) tại các thụ thể amylin và calcitonin, tương ứng, so với petrelintide. Hoạt chất này cũng cho thấy giảm cân phụ thuộc liều trong khoảng liều 0,012 - 0,12 mg/kg trên mô hình chuột béo phì do ăn uống (DIO).
Tại liều 0,04 mg/kg, BGM1812 đạt được mức giảm cân lớn hơn so với petrelintide, một sản phẩm đang được Zealand Pharma phát triển. Ngoài ra, BGM1812 duy trì đáng kể khối lượng nạc tương đối trong khi giảm khối lượng mỡ tương đối. Bên cạnh đó, sự kết hợp giữa BGM1812 và BGM0504 dẫn đến giảm cân nhiều hơn và kéo dài hơn so với cả semaglutide+cagrilintide hoặc amycretin trong mô hình chuột DIO.
Về BGM0504
Thuốc hạ đường huyết dạng peptid BGM0504 là một chất kích thích kép của các thụ thể GLP-1 (glucagon-like peptide 1) và GIP (glucose-dependent insulinotropic polypeptide), được BrightGene phát triển độc lập. BGM0504 có thể kích hoạt các con đường dẫn truyền tín hiệu của GIP và GLP-1, tạo ra các hiệu ứng sinh học như kiểm soát đường huyết, giảm cân và điều trị viêm gan nhiễm mỡ không do rượu (NASH), đồng thời cho thấy tiềm năng trong điều trị nhiều bệnh chuyển hóa. Hiện BGM0504 đang trong giai đoạn thử nghiệm lâm sàng giai đoạn 3 tại Trung Quốc để quản lý cân nặng và bệnh tiểu đường loại 2, đồng thời đã hoàn tất nghiên cứu giai đoạn 1 tại Mỹ cho chỉ định quản lý cân nặng. Tính đến nay, BGM0504 đã được nghiên cứu trên hơn 1.000 bệnh nhân và cho thấy hiệu quả vượt trội cùng hồ sơ an toàn mạnh mẽ.
Về BGM1812
BGM1812 là một analog amylin mới, được thiết kế thông qua tối ưu hóa sử dụng AI/ML nhằm tăng cường hoạt tính kích thích và đặc tính công thức. Là một loại amylin mạnh và có tác dụng kéo dài đặc biệt, BGM1812 có tiềm năng trở thành viên thuốc uống dùng hàng tuần.
Về BrightGene
BrightGene là một công ty dược phẩm quốc tế định hướng đổi mới, niêm yết trên Sở giao dịch chứng khoán Thượng Hải, chuyên phát triển và sản xuất các liệu pháp điều trị chất lượng cao để đáp ứng nhu cầu chưa được thỏa mãn của bệnh nhân. Được thành lập vào năm 2001, BrightGene đã phát triển từ một nhà lãnh đạo toàn cầu trong lĩnh vực biệt dược và sinh phẩm tương tự có rào cản cao trở thành nhà phát triển các liệu pháp điều trị chuyển hóa và hô hấp tiên tiến. Là một đơn vị dẫn đầu trong lĩnh vực hóa học phức tạp và liên hợp, BrightGene sở hữu các nền tảng tiên tiến độc quyền trong lĩnh vực peptid, siRNA, nanobody, cũng như các công thức tiên tiến, và có 272 bằng sáng chế. Công ty vẫn là nhà cung cấp toàn cầu cho 15 API và 2 sản phẩm thuốc tại Mỹ và EU. Trụ sở chính của BrightGene đặt tại Trung Quốc. Thông tin thêm có thể tìm thấy tại https://www.bright-gene.com/.

nguồn: Bright Gene Related Stocks: Shanghai:688166 Shanghai:688166.SS